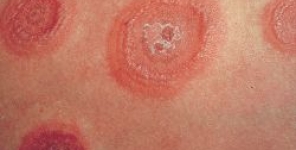
Vemurafenib: un'insolita fotosensibilità indotta dagli UVA
 Vemurafenib è una nuova terapia mirata approvata per il trattamento di pazienti con mutante BRAF V600E del melanoma metastatico.
Vemurafenib è una nuova terapia mirata approvata per il trattamento di pazienti con mutante BRAF V600E del melanoma metastatico.
Tra gli eventi avversi cutanei che sono stati riportati, è spesso sperimentata la fotosensibilità. Abbiamo voluto caratterizzare più approfonditamente il meccanismo che porta a questa fotosensibilità e il corrispondente spettro UV.
I foto-test hanno mostrato che la fototossicità è stata dipendente dagli UVA a partire dal valore normale prima del trattamento vemurafenib, la dose minima di UVA per l'eritema è diminuita in 17 pazienti su 18 (94.4%), mentre la dose minima per l'eritema è rimasta invariata. Inoltre, un eritema indotto dal vemurafenib è apparso rapidamente durante l'esposizione UVA, contrariamente a quello che si osservava con una convenzionale fototossicità indotta dai farmaci, la quale mostrava un eritema 12-24 ore dopo il foto-test. La concentrazione di vitamina PP è diminuita, e il livello di porfirina è aumentato significativamente dopo 2 mesi di vemurafenib.
Il nostro studio conferma l'elevato rischio di fotosensibilità indotta da vemurafenib e indica che forse è dipendente dalla vitamina PP e dalla porfirina.
Storia della pubblicazione:
Titolo: Vemurafenib: an unusual UVA-induced photosensitivity
Rivista: Experimental Dermatology. doi: 10.1111/exd.12119
Autori: Pauline Gelot, Hervé Dutartre, Amir Khammari, Aurélie Boisrobert, Caroline Schmitt, Jean-Charles Deybach, Jean-Michel Nguyen, Sophie Seité, Brigitte Dréno
Affiliazioni:Oncodermatology Unit, CHU Hotel Dieu, Nantes, France Inserm U-CNRS U, CIC Biothérapie Inserm , Nantes, France Centre Français des Porphyries, Service de Biochimie, Hôpital Louis Mourier, APHP, Colombes, France Inserm U, Centre de Recherche Biomédicale Bichat Beaujon CRB, Université Paris Diderot, site Bichat, Paris, France Epidemiology and Biostatistics Unit, CHU Nantes, France La Roche-Posay Pharmaceutical Laboratories, Asnières, France
Abstract:
Vemurafenib is a new-targeted therapy approved for the treatment of patients with V600E BRAF-mutant metastatic melanoma. Among the cutaneous adverse events reported, the photosensitivity is frequently experienced. We aimed to characterize more deeply the mechanism leading to this photosensitivity as well as the corresponding UV spectrum. Phototests showed that the phototoxicity was UVA-dependent since from normal value prior to vemurafenib treatment, the UVA-minimal erythema dose decreased in 17 of 18 patients (94.4%) while the minimal erythema dose remained unchanged. Furthermore, a vemurafenib-induced erythema appeared quickly during the UVA exposure contrarily to what is observed with a conventional drug-induced phototoxicity showing an erythema 12–24 h after the phototesting. Vitamin PP concentration decreased, and porphyrin level significantly increased after 2 months of vemurafenib. Our study confirms the high risk of vemurafenib-induced photosensitivity and indicates that it is possibly vitamin PP- and porphyrin dependent.