Un nuovo test capace di identificare il rischio metastatico dei melanomi al primo stadio
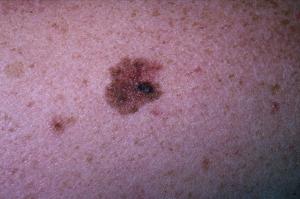 Due terzi dei pazienti affetti da melanoma che successivamente sono soggetti a metastasi o muoiono, ricevono una diagnosi durante il primo stadio della malattia, perciò è importante determinare il rischio di metastasi nei pazienti con melanoma al primo stadio. Circa il 75% dei pazienti affetti da melanoma viene diagnosticato durante i primi stadi della malattia (stadio I o II).
Due terzi dei pazienti affetti da melanoma che successivamente sono soggetti a metastasi o muoiono, ricevono una diagnosi durante il primo stadio della malattia, perciò è importante determinare il rischio di metastasi nei pazienti con melanoma al primo stadio. Circa il 75% dei pazienti affetti da melanoma viene diagnosticato durante i primi stadi della malattia (stadio I o II).
Secondo uno studio pubblicato nel numero di Gennaio di Clinical Cancer Research, un nuovo strumento prognostico basato su una firma genetica a 28 geni (DecisionDx-Melanoma, Castle Biosciences) potrebbe essere in grado di prevedere quali pazienti affetti da melanoma allo stadio I o II, sono ad alto rischio di metastasi e potrebbe influenzare il trattamento clinico di questi pazienti.
La firma a 28 geni è predittiva del rischio del paziente di sviluppare metastasi, indipendentemente da fattori quali la posizione nel sistema di classificazione del melanoma del Joint Committee on Cancer (AJCC), lo spessore di Breslow , la presenza di ulcerazioni, tasso mitotico ed età.
"Il comportamento dei melanomi è molto variabile e spesso non può essere pronosticato con precisione tramite i tradizionali sistemi di classificazione", ha dichiarato in un comunicato stampa l'autore dello studio Pedram Gerami, professore di dermatologia e direttore del programma di ricerca sul melanoma dell'istituto di ricerca sul cancro della Northwestern University di Chicago.
"Questi risultati dimostrano che una firma genetica può prevedere con precisione il rischio di metastasi, soprattutto in tumori classificati come a basso rischio metastatico a causa di fattori come lo stadio della malattia, le dimensioni ed altre caratteristiche. Il test potrebbe avere un significativo impatto sul piano clinico e sui risultati a lungo termine del trattamento di questi pazienti", ha aggiunto.
"Il set di dati proposti a sostegno del metodo basato sulla firma a 28 geni è ridotto, ma i dati sono convincenti" ha dichiarato Jeffrey J. Sussman, professore di chirurgia e direttore della divisione di oncologia chirugica presso la School of Medicine della Cincinnati University e non coinvolto nello studio che nel corso della propria pratica clinica impiega questo tipo di test su pazienti con linfonodo negativo e con fattori di rischio più elevato (fase IIa/IIb).
Nello studio, i pattern di espressione genica (GEP) sono stati analizzati in campioni fissati in formalina e inclusi in paraffina ottenuti da biopsie o procedure di escissione di melanomi primitivi.
L'RNA dei campioni è stato convertito in DNA complementare, amplificato e caricato su un chip contenente "28 geni discriminanti bersaglio" e tre geni di controllo.
I 28 geni sono stati selezionati a partire da banche dati pubbliche di melanomi primitivi; la società ha effettuato analisi accurate per identificare i geni che potrebbero indicare una malattia ad alto rischio di metastasi ed ha scoperto che, nel melanoma aggressivo, alcuni di questi geni sono sovraregolati mentre alti sono sottoregolati.
I GEP sono stati usati per classificare pazienti con melanoma di stadio I o II come a basso rischio (classe 1) o ad altro rischio (classe 2).
La firma a 28 geni è stata stabilita in coorti di sviluppo e di formazione ed è stata convalidata in una coorte indipendente composta da 104 pazienti, 35 dei quali hanno sviluppato condizioni metastatiche. Il tempo di follow-up per i pazienti che non hanno sviluppato metastasi è stato di 7,3 anni.
Nella coorte di validazione, 61 pazienti sono stati classificati come aventi un GEP a basso rischio, mentre 43 sono stati classificati ad alto rischio.
La sopravvivenza a cinque anni in assenza di malattia, era significativamente migliore per i pazienti a basso rischio nella coorte che per quelli ad alto rischio (97% contro 31%, P < .0001); questo confronto si allinea con i tassi a 5 anni visti nella coorte di sviluppo (100% contro 38%).
Quando le coorti di sviluppo e di validazione sono state combinate (n=220), i GEP hanno identificato con precisione il 90% dei pazienti senza prova documentata di metastasi e l'80% di quelli con metastasi documentata.
Il metodo con firma a 28 geni è stato convalidato in modo indipendente in una coorte di 217 pazienti con biopsia del linfonodo sentinella negativo, ha dichiarato Derek Maetzold, presidente e CEO di Castle Biosciences. Egli ha inoltre riferito che lo studio di questa coorte di validazione è attualmente in fase di pubblicazione.
Cambiamenti nella gestione clinica dei pazienti
Il test a 28 geni ha mostrato una significativa capacità di identificare con precisione i pazienti ad alto rischio metastasi e di conseguenza il tasso di mortalità, ha dichiarato il Dr. Gerami. Il sistema di classificazione AJCC ha dei limiti: due terzi dei pazienti che muoiono sono inizialmente diagnosticati con melanomi allo stadio I o II e non vengono classificati come ad alto rischio sull abase della biopsia del linfonodo sentinella, ha proseguito. La firma a 28 geni potrebbe cambiare la gestione clinica dei pazienti con melanoma in stadio precoce: i pazienti con malattia in stadio I e II sono in genere seguiti in cliniche dermatologiche o generiche, dove vengono sottoposti ad esami della pelle ma non al rigoroso protocollo di imaging dei pazienti con melanoma al III stadio. Tuttavia, ora che ci sono nuove opzioni di trattamento per il melanoma, l'identificazione dei pazienti ad alto rischio di metastasi è importantissima, ha detto il Dr. Gerami.
"I pazienti che presentano una firma ad alto rischio possono essere monitorati più frequentemente e sottoposti ad ulteriori test per individuare le metastasi al più presto", ha detto Alexander Miller, chirugo oncologico specializzato in cancro al seno e melanoma della South Texas Oncology and Hematology di San Antonio, che usa regolarmente il test.
Commercializzazione del test
"Castle Biosciences ha dato il via agli ordini per questo test nel 2013, dopo il completamento dei primi due stadi di valutazione clinica" ha dichiarato Maetzold. "Il test viene ordinato principalmente da chirurghi e dermatologi per migliorare la gestione di pazienti con diagnosi di malattia in stadio precoce" ha spiegato. "I chirurghi oncologici utilizzano il test principalment eper monitorare adeguatament ei paziente un biopsia del linfonodo sentinella negativo" ha aggiunto.
Maetzold ha anche fatto notare che i dati degli studi clinici dimostrano che ilt esto non è indicato per paziente con linfonodo positivo o con malattia in stadio III. Ha però dichiarato che spera che i primi due studi forniscano prove sufficienti per la commissione NCCN a considerare l'inclusione del test nelle future linee guida per la pratica clinica ed il monitoraggio dei pazienti che non sono considerati a rischio sulla base dei criteri di classificazione tradizionali. Maetzold pensa che il test dovrebbe essere impiegato in tutti i pazienti con melanoma allo stadio I o II.
Riferimenti:
Clin Cancer Res. 2015;21(1):175-183.