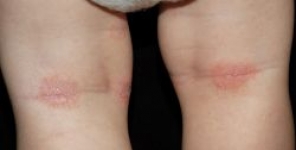
FDA approva il crisaborolo per il trattamento della dermatite atopica
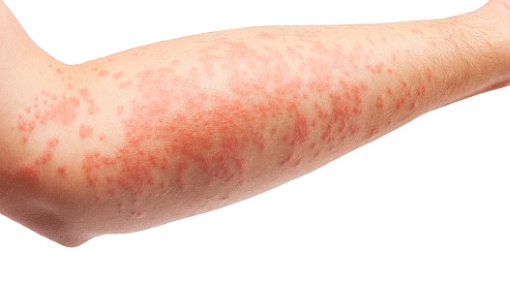
L'agenzia americana per il farmaco FDA ha approvato il crisaborolo (Eucrisa, Pfizer Inc.) per il trattamento della dermatite atopica (eczema) da lieve a moderata nei pazienti di età pari o superiore ai 2 anni.
"Questa approvazione mette a disposizione dei pazienti con dermatite atopica una nuova opzione di trattamento", ha dichiarato in un comunicato stampa Amy Egan, vice direttore del dipartimento Drug Evaluation III del centro di ricerca FDA.
Il crisaborolo è un inibitore delle fosfodiesterasi PDE-4 che va applicato due volte al giorno; al momento il suo specifico meccanismo di azione nel quadro della dermatite atopica è ancora sconosciuto.
L'approvazione poggia sulla valutazione dei risultati di due studi controllati contro placebo. Gli studi hanno coinvolto un totale di 1522 pazienti di età compresa fra i 2 e i 79 anni, con dermatite atopica lieve o moderata. I pazienti trattati con crisaborolo hanno raggiunto la scomparsa totale o parziale dell'eczema dopo 28 giorni di trattamento.
Gli eventi avversi di natura più grave riguardano i soggetti con ipersensibilità al principio attivo impiegato. Gli eventi avversi più frequenti sono dolore e bruciore al sito di iniezione.