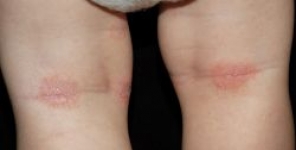
Caratterizzazione dell'espressione di EGFR e ErbB2 in pazienti affetti da dermatite atopica
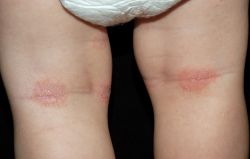 La dermatite atopica (AD) è una delle malattie infiammatorie croniche più comuni della pelle nei paesi industrializzati. Per identificare i geni candidati coinvolti nella patogenesi di AD, abbiamo prima intrapreso un approccio genomico ampio utilizzando DNA microarray.
La dermatite atopica (AD) è una delle malattie infiammatorie croniche più comuni della pelle nei paesi industrializzati. Per identificare i geni candidati coinvolti nella patogenesi di AD, abbiamo prima intrapreso un approccio genomico ampio utilizzando DNA microarray.
Un trascritto che codifica il recettore del fattore di crescita epidermico (EGFR), è risultato essere tra i trascritti sotto-regolati nella pelle AD. Qui, abbiamo ulteriormente studiato il modello di espressione dei due membri della famiglia EGFR (EGFR ed ErbB2) in pelle AD a livello proteico. L'analisi immunoistochimica (IHC) di EGFR ed ErbB2 ha mostrato una diminuita espressione delle proteine EGFR ed ErbB2 nella pelle AD lesionata rispetto alla pelle di individui sani.
In modo interessante, abbiamo scoperto che EGFR e ErbB2 sono reciprocamente espressi in un modello in vitro di proliferazione e differenziazione dei cheratinociti, mettendo in parallelo i profili di espressione trovati nell'epidermide di pelle sana. I massimi livelli di trascritti di EGFR sono stati trovati nelle cellule proliferanti, mentre ErbB2 è stato trovato in cellule differenziate. Abbiamo dimostrato che bloccando l'attività di EGFR combinata con la co-stimolazione della citochina Th2 IL4 nei cheratinociti conduce all'induzione della chemochina infiammatoria CCL26/eotaxina-3 in vitro.
Di conseguenza, l'aumento dei livelli trascrizionali di CCL26 sono stati osservati nella pelle AD lesionata. Presi insieme, la soppressione di EGFR può contribuire alla patogenesi di AD mediante la regolazione delle chemochine infiammatorie.
Fonte:
Titolo: Characterization of EGFR and ErbB2 expression in atopic dermatitis patients
Rivista: Archives of Dermatological Research. doi: 10.1007/s00403-012-1242-4
Autori: Annika Sääf, Andor Pivarcsi, Mårten C. G. Winge, Carl-Fredrik Wahlgren, Bernhard Homey, Magnus Nordenskjöld, Maria Tengvall-Linder, Maria Bradley
Affiliazioni: Institute of Environmental Medicine, Karolinska Institutet, Stockholm, Sweden
Department of Medicine Solna, Dermatology and Venereology Unit, Karolinska Institutet, Stockholm, Sweden
Department of Medicine Solna, Dermatology Unit, Karolinska Institutet and Karolinska University Hospital, Stockholm, Sweden
Department of Molecular Medicine and Surgery, Center for Molecular Medicine, Karolinska Institutet, Stockholm, Sweden
Department of Dermatology, University Hospital, Düsseldorf, Germany
Department of Medicine Solna, Clinical Immunology and Allergy, Karolinska Institutet, Stockholm, Sweden
Abstract:
Atopic dermatitis (AD) is one of the most common chronic inflammatory skin diseases in industrialized countries. To identify candidate genes involved in the pathogenesis of AD, we previously undertook a genome-wide approach using DNA microarrays. A transcript encoding the epidermal growth factor receptor (EGFR) was found to be among the down-regulated transcripts in AD skin. Here, we further investigated the expression pattern of two EGFR family members (EGFR and ErbB2) in AD skin on a protein level. Immunohistochemical (IHC) analysis of EGFR and ErbB2 showed decreased expression of EGFR and ErbB2 proteins in AD lesional skin as compared to skin from healthy individuals. Interestingly, we found that EGFR and ErbB2 were reciprocally expressed in an in vitro model of keratinocyte proliferation and differentiation, paralleling the expression patterns found in epidermis of healthy skin. The highest levels of EGFR transcripts were found in proliferating cells, while ErbB2 was found in differentiated cells. We show that blocking EGFR activity combined with co-stimulation of the Th2-cytokine IL4 in keratinocytes leads to induction of the inflammatory chemokine CCL26/eotaxin-3 in vitro. Accordingly, increased CCL26 transcriptional levels were observed in AD lesional skin. Taken together, suppression of EGFR may contribute to the pathogenesis of AD via the regulation of inflammatory chemokines.