Trattamento con bimatoprost per l'ipotricosi delle sopracciglia: uno studio pilota randomizzato, in doppio cieco e controllato
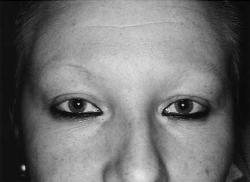 La Food and Drug Administration ha approvato la soluzione oftalmica di bimatoprost (0.03%) per il trattamento dell'ipotricosi delle ciglia; mentre rimangono perlopiù aneddotici gli studi riguardo l'efficacia di questo farmaco sulle sopracciglia.
La Food and Drug Administration ha approvato la soluzione oftalmica di bimatoprost (0.03%) per il trattamento dell'ipotricosi delle ciglia; mentre rimangono perlopiù aneddotici gli studi riguardo l'efficacia di questo farmaco sulle sopracciglia.
Obiettivo
Valutare l'efficacia e la sicurezza della soluzione oftalmica di bimatoprost 0.03% applicata sulle sopracciglia attraverso uno studio randomizzato, in doppio cieco e controllato con veicolo. Metodi Nello studio sono stati inclusi i soggetti (n = 20) con ipotricosi delle sopracciglia da lieve a moderata. Un gruppo (Bim) ha applicato il bimatoprost su ciascun sopracciglio, una volta al giorno per 9 mesi; mentre i soggetti dell'altro gruppo hanno applicato il veicolo su ciascun sopracciglio, ogni notte per 5 mesi. I soggetti del secondo gruppo sono stati nuovamente randomizzati per applicare il bimatoprost (gruppo Veh-Bim) o il veicolo (gruppo Veh) su ciascun sopracciglio, una volta al giorno per 4 mesi. L'end point primario è stato definito come l'aspetto del sopracciglio alla valutazione dallo sperimentatore, mentre gli end point secondari sono stati i risultati riportati dai pazienti.
Risultati
Le valutazioni degli osservatori hanno mostrato dei miglioramenti significativi dopo 6 (p = .002) e 7 mesi (p = .005), rispetto al basale, per quanto riguarda le sopracciglia trattate con bimatoprost. In nessun momento, i valori-p per il gruppo Veh-Bim e per quello Veh sono risultati significativi. La soddisfazione dei soggetti alla fine dello studio — per quanto riguarda la pienezza, lo spessore o il colore delle sopracciglia — è stata maggiore nel gruppo Bim rispetto al gruppo Veh. Inoltre, non sono stati osservati effetti avversi.
Conclusione
La soluzione oftalmica di bimatoprost allo 0.03%, applicata quotidianamente per 9 mesi, migliora l'aspetto delle sopracciglia molto più del veicolo e non presenta effetti collaterali.
Storia della pubblicazione:
Titolo: Treatment of Eyebrow Hypotrichosis Using Bimatoprost: A Randomized, Double-Blind, Vehicle-Controlled Pilot Study
Rivista: Dermatologic Surgery. doi: 10.1111/dsu.12199
Autori: Kenneth R. Beer, Hillary Julius, Monica Dunn, Fred Wilson
Affiliazioni:Kenneth Beer MD PA General, Esthetic and Surgical Dermatology, West Palm Beach, Florida WilWrite LLC, Camillus, New York
Abstract:
Background The Food and Drug Administration has approved bimatoprost ophthalmic solution (0.03%) for the treatment of eyelash hypotrichosis. Previous reports of its efficacy in eyebrow hypotrichosis are anecdotal. Objective To assess the efficacy and safety of bimatoprost 0.03% ophthalmic solution applied to the eyebrows in a randomized, double-blind, vehicle-controlled study. Methods Subjects (n = 20) with mild to moderate eyebrow hypotrichosis enrolled in the study. One group (Bim) applied bimatoprost to each eyebrow daily for 9 months, and another applied vehicle nightly to each eyebrow for 5 months. Subjects in the latter group were re-randomized to apply bimatoprost (Veh-Bim Group) or vehicle (Veh Group) daily to each eyebrow for 4 months. The primary end point was investigator-assessed eyebrow appearance; secondary end points were subject-reported outcomes. Results Investigator assessments showed significant improvements from baseline to 6 (p = .002) and 7 (p = .005) months for the eyebrows treated with bimatoprost. p-Values for the Veh-Bim and Veh groups were not significant at any time point. End-of-study subject satisfaction with eyebrow fullness or thickness and darkness or color was greater in the Bim group than in the Veh group. Adverse effects were not observed. Conclusion Bimatoprost 0.03% ophthalmic solution applied daily for 9 months improves the appearance of eyebrows noticeably more than vehicle, without side effects.