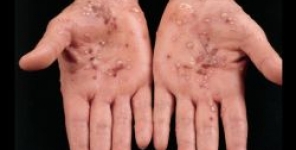
Psoriasi: Guselkumab si mostra promettente

Guselkumab, un anticorpo monoclonale anti-interleuchina-23, ha ottenuto risultati significativamente superiori rispetto alla terapia a base di adalimumab nel trattamento della psoriasi a placche.
I risultati dello studio randomizzato di fase 2, controllato contro placebo, sono stati pubblicati nel New England Journal of Medicine. Gli esperti richiamano alla cautela, facendo notare come siano ancora necessari ulteriori dati per poter valutare accuratamente il profilo di sicurezza del farmaco.
Alla settimana 16 dello studio multi-sito i pazienti che hanno ricevuto 50 mg o più di guselkumab hanno mostrato la migliore risposta clinica; dosi più alte hanno portato un numero maggiore di pazienti a raggiungere punteggi pari a 0, che corrisponde a una completa risoluzione della psoriasi, o pari a 1, che corrisponde a una psoriasi lieve, rispetto all'indice Physician's Global Assessment (PGA). I risultati migliori sono stati osservati nei pazienti trattati con 100 mg ogni 8 settimane, l'86% di questi pazienti ha ottenuto un punteggio pari a 0 o 1 rispetto all'indice PGA. Fra i pazienti nel gruppo Adalimumab il 58% ha raggiunto un punteggio di 0 o 1 dopo 16 settimane mentre solo il 7% dei pazienti nel gruppo placebo ha raggiunto punteggi simili (P ≤ .002).
"Guselkumab ha un'efficacia maggiore rispetto ad adalimumab e ha un meccanismo d'azione più specificamente mirato alla psoriasi rispetto a ustekinumab" scrivono gli autori dello studio. "Per esaminare la sicurezza e l'efficacia di guselkumab per il trattamento della psoriasi da moderata a grave sono in corso studi di fase 3 di maggiore durata e che coinvolgono un numero maggiore di pazienti."
Uno studio randomizzato durato 52 settimane
Il Dr. Kenneth B. Gordon, professore presso il dipartimento di Dermatologia della Feinberg School of Medicine di Chicago, e colleghi hanno condotto su 293 pazienti uno studio randomizzato in doppio cieco, della durata di 52 settimane per comparare guselkumab (CNTO 1959), un anticorpo monoclonale anti-interleuchina-23 con adalimumab, un anticorpo monoclonale contro il fattore di necrosi tumorale, e contro placebo. Lo studio ha adottato una definizione di psoriasi a placche da moderata a grave che si basa sull'interessamento di almeno il 10% della superficie dermica totale, oltre a un punteggio PGA di 3 o superiore e a un punteggio di 12 o più rispetto allo Psoriasis Area and Severity Index.
L'endpoint primario era la percentuale di pazienti con un punteggio PGA di 0 o 1 alla settimana 16.
Per le prime 40 settimane, 43 pazienti sono stati assegnati in modo casuale a una dose standard di adalimumab (80 mg alla settimana 0 e 40 mg settimana 1 e poi ogni due settimane fino alla settimana 39), 42 pazienti sono stati assegnati al gruppo placebo e 208 pazienti sono stati assegnati al gruppo guselkumab. I ricercatori hanno assegnato in modo casuale i pazienti nel gruppo guselkumab a vari dosaggi del farmaco: 5 mg a settimana per le prime 4 settimane ed in seguito ogni 12 settimane (41 pazienti), 15 mg ogni 8 settimane (41 pazienti), 50 mg a settimana fino alla settimana 4 e successivamente ogni 12 settimane (42 pazienti), 100 mg ogni 8 settimane (42 pazienti), o 200 mg a settimana fino alla settimana 4 e successivamente ogni 12 settimane (42 pazienti). Alla settimana 16, i pazienti nel gruppo placebo hanno ricevuto 100 mg guselkumab ogni 8 settimane. La somministrazione di adalimumab non si è verificata in cieco, ma l'incaricato delle valutazioni non era a conoscenza delle assegnazioni rispetto ai gruppi.
Alla settimana 40, la percentuale di pazienti con un punteggio PGA di 0 o 1 è stata superiore nei gruppi guselkumab con dosaggio pari a 50 mg (71%), 100 mg (77%), e 200 mg (81%) rispetto al gruppo adalimumab (49% ; P <.05), e maggiore nei gruppi guselkumab (a qualsiasi dosaggio) rispetto al gruppo placebo. La maggior parte dei pazienti nel gruppo guselkumab con dosaggio pari a 100 mg ha ottenuto una completa remissione della psoriasi, il 62% dei pazienti ha ottenuto un un punteggio PGA di 0 e un miglioramento del 100% rispetto alla baseline secondo lo Psoriasis Area and Severity Index.
L'efficacia di guselkumab è leggermente diminuita verso la fine della terapia nei gruppi con dosaggio a 12 settimane, rispetto ai pazienti con dosaggio a 8 settimane.
Ancora troppo presto per parlare di sicurezza
"Si tratta di un farmaco interessante," ha dichiarato il Dr. Guy Webster, professore presso il dipartimento di Dermatologia del Jefferson Medical College di Philadelphia. "Lo studio è stato ben condotto" ha detto, "ma è troppo presto per giudicare la sicurezza del farmaco". "Quello che abbiamo a disposizione è un piccolo studio di fase 2, e quello che sembra un profilo di sicurezza promettente potrebbe rivelarsi molto diverso nel contesto di un'assunzione a lungo termine da parte di un numero maggiore di soggetti. Basta ricordare come Raptiva (di Genentech) sembrasse sicuro, nei primi anni dopo la sua introduzione sul mercato".
"Sembra molto più efficace di adalimumab per la psoriasi, almeno stando ai dati di questo piccolo studio ma la sua efficacia è elevata al punto da compensare per il rischio di eventi avversi ancora ignoti? Si tratta di una decisione difficile", ha continuato il Dr. Webster. "Adalimumab è un buon farmaco con una lunga storia di sicurezza, che viene assunto attualmente da molti pazienti", ha detto. "Sicuramente sarà presto condotto uno studio più grande e allora vedremo se i risultati e il profilo di sicurezza verranno confermati".
Alla settimana 16, l'incidenza di eventi avversi è stata simile nei tre gruppi di trattamento: 52% nel gruppo placebo, 50% nei gruppi guselkumab e 56% nel gruppo adalimumab. I ricercatori notano anche come non siano emerse prove a sostegno di una relazione dose-risposta nel tasso di eventi avversi dei gruppi assegnati alla terapia con guselkumab. Il 20% dei pazienti nei gruppi guselkumab ha avuto infezioni nelle prime 16 settimane rispetto al solo 12% del gruppo Adalimumab e al 14% nel gruppo placebo. I tassi di infezione per guselkumab e adalimumab sono risultati simili nelle settimane da 16 a 52, con infezioni osservate nel 30% dei soggetti dei gruppi guselkumab e nel 37% dei soggetti del gruppo adalimumab.
Nelle settimane da 16 a 52, i pazienti nel gruppo adalimumab hanno avuto una percentuale leggermente superiore di eventi avversi rispetto a quelli dei gruppi guselkumab (61% vs 49%). L'infezione è stata l'evento avverso più comunemente riportato nel corso dello studio ed è stata osservata in circa il 30% dei pazienti. Nessun paziente nei gruppi guselkumab ha riportato infezioni gravi, nel gruppo adalimumab solo un paziente è stato interessato da un'infezione di grave entità.
Nei gruppi guselkumab 3 dei 235 pazienti hanno interrotto il trattamento a causa degli eventi avversi manifestatisi nel corso delle prime 40 settimane, mentre un solo paziente ha interrotto il trattamento nel gruppo adalimumab. Nei gruppi guselkumab quattro pazienti hanno manifestato eventi avversi di grave entità, rispetto a uno del gruppo adalimumab.
Gli autori hanno tenuto a sottolineare come il campione relativamente piccolo nei diversi gruppi di trattamento sia stata una limitazione alla portata dello studio. Inoltre, le caratteristiche al basale dei pazienti non sono state bilanciate tra i gruppi.
Riferimenti:
New England Journal of Medicine. 2015;373:136-144. Abstract