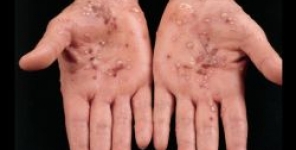
FDA approva ixekizumab per la psoriasi a placche

L'agenzia americana per il farmaco FDA ha approvato ixekizumab (Taltz, Eli Lilly) per il trattamento della psoriasi a placche da moderata a severa negli adulti.
Ixekizumab è un anticorpo monoclonale umanizzato che ha come bersaglio l'interleuchina 17A, responsabile dei processi infiammatori legati alla psoriasi. Ixekizumab viene somministrato tramite iniezione ed è rivolto ai pazienti soddisfano i criteri necessari per la terapia sistemica, per la fototerapia o una combinazione di entrambe.
"Questa approvazione fornisce ai pazienti con psoriasi a placche un'opzione di trattamento importante per contribuire ad alleviare l'irritazione della pelle e il disagio provocato da questa condizione", ha spiegato la Dr.ssa Julie Beitz, direttrice del dipartimento di Valutazione dei Farmaci del centro di ricerca della FDA.
La sicurezza e l'efficacia di ixekizumab sono state dimostrate in tre studi randomizzati e controllati contro placebo, che hanno coinvolto oltre 3.800 pazienti con psoriasi a placche.
I risultati di questi studi hanno evidenziato che ixekizumab è in grado di produrre una "maggiore risposta clinica rispetto al placebo, con una risoluzione totale o quasi totale, valutata in termini di estensione, natura e gravità delle manifestazioni cutanee", questo quanto dichiarato da FDA nel comunicato stampa relativo all'approvazione.
Poiché la terapia con ixekizumab rientra nelle immunoterapie, il comunicato chiarisce che l'impiego del farmaco è condizionale all'informazione del paziente circa il maggior rischio di infezione e il rischio di una reazione allergica o autoimmune legati all'assunzione del farmaco.
Gli effetti collaterali più comuni sono: infezioni del tratto respiratorio superiore, reazioni al sito d'iniezione e infezioni di natura micotica (tinea). FDA ha anche fatto sapere che ci sono stati casi di reazione allergica, nonché di comparsa o peggioramento della sindrome del colon irritabile, perciò i pazienti in terapia con ixekizumab dovrebbero essere monitorati con attenzione per questo tipo di effetti collaterali.
Il mese scorso, il dipartimento per i medicinali ad uso umano dell'agenzia europea per il farmaco (European Medicines Agency) ha raccomandato la commercializzazione di ixekizumab per l'impiego nei pazienti adulti con psoriasi a placche da moderata a severa che sono buoni candidati per la terapia sistemica.
La psoriasi interessa 125 milioni di persone al mondo e il 20% di queste, secondo Eli Lilly, è affetto da psoriasi a placche da moderata a severa.