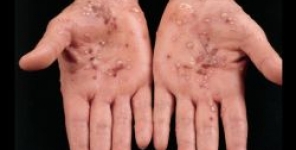
FDA approva guselkumab per la psoriasi a placche

In un comunicato stampa dell'azienda produttrice, è stata resa pubblica l'approvazione di guselkumab (Tremfya, Janssen Biotech) da parte dell'agenzia americana per il farmaco; guselkumab è stato approvato per gli adulti con psoriasi a placche da moderata a grave, che si sono rivelati buoni candidati per la terapia sistemica o per la fototerapia.
L'azienda ha sottolineato che al momento guselkumab è il primo e l'unico agente biologico approvato da FDA che blocca selettivamente IL-23, interleuchina che gioca un ruolo chiave nella psoriasi a placche. L'anticorpo monoclonale viene somministrato sotto forma di iniezione sottocutanea in dosi da 100 mg ogni otto settimane, dopo una somministrazione iniziale alla settimana 0 e alla settimana 4.
Guselkumab rappresenta una "pietra miliare nel trattamento della psoriasi a placche da moderata a severa, come dimostrato dalla clearance raggiunta nella maggior parte degli studi su pazienti in terapia con il farmaco", ha sottolineato nel comunicato il Dr. Andrew Blauvelt, presidente dell'Oregon Medical Research Center di Portland.
"Continuiamo a fare progressi nella comprensione della fisiopatologia della psoriasi e del ruolo giocato da IL-23 nella patogenesi della malattia. Per questo, come ricercatore e come dermatologo, trovo che l'approvazione di guselkumab sia un traguardo molto importante", ha aggiunto.
FDA ha approvato guselkumab sulla base dei risultati ottenuti dal programma di sviluppo che ha coinvolto oltre 2.000 pazienti in tre studi di fase 3.
Alla sedicesima settimana di terapia, almeno 7 su 10 pazienti trattati con guselkumab hanno raggiunto una clearance del 90% (Psoriasis Area and Severity Index, PASI 90) e oltre l'80% ha mostrato significativi miglioramenti in termini di lesioni. I pazienti che hanno raggiunto un punteggio PASI pari a 90 alla 28° settimana di trattamento, hanno mantenuto i risultati fino alla 48° settimana.
Guselkumab ha dato miglioramenti anche nei casi di coinvolgimento del cuoio capelluto e ha influito positivamente sui sintomi della psoriasi a placche (prurito, dolore, sensazione di bruciore e secchezza cutanea) alla 16° settimana di trattamento.
Guselkumab si è dimostrato in grado di ottenere risultati migliori, in termini di clearance cutanea, rispetto a adalimumab (Humira, AbbVie) in uno studio che ha confrontato i due farmaci alla 16°, 24° e 48° settimana di terapia. Guselkumab si è mostrato efficace anche in quei pazienti che avevano esibito una risposta inadeguata alla terapia con ustekinumab (Stelara, Janssen Biotech).
Il Dr. Michael Siegel, vice presidente del programma di ricerca della National Psoriasis Foundation, ha commentato così la notizia: "L'approvazione di nuove opzioni di trattamento sicure ed efficaci è sempre un'ottima notizia per la comunità di pazienti affetti da psoriasi a placche, poiché non tutti i pazienti rispondono alle terapie attualmente disponibili. Per molti pazienti con psoriasi a placche da moderata a grave, l'approvazione di guselkumab rappresenta un'importante aggiunta all'arsenale medico e offre a dermatologi e pazienti una terapia che inibisca selettivamente IL-23."