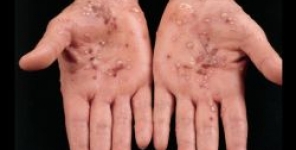
L'Unione europea approva brodalumab per la psoriasi a placche

In un comunicato stampa, AstraZeneca e Medimmune annunciano che brodalumab (Kyntheum, LEO Pharma, A/S) è stato approvato dall'Unione europea per il trattamento della psoriasi a placche da moderata a severa negli adulti idonei alla terapia sistemica.
Brodalumab inibisce selettivamente il recettore di IL-17, bloccando così la risposta infiammatoria coinvolta nella psoriasi a placche.
L'approvazione da parte della Comunità europea avviene a seguito di una raccomandazione positiva del comitato per i farmaci a uso umano (CHMP) dell'agenzia europea per il farmaco (EMA) e risalente a maggio 2017.
Brodalumab è stato valutato nel corso di tre studi clinici randomizzati e controllati (AMAGINE 1-3) che hanno coinvolto oltre 4.300 pazienti.
Negli studi AMAGINE-2 e AMAGINE-3, più pazienti trattati con brodalumab che pazienti trattati con ustekinumab hanno raggiunto un tasso di risposta, rispetto allo Psoriasis Area Severity Index (PASI), di 100 dopo 12 settimane (44% contro 22% in AMAGINE-2 e 37% contro 19% in AMAGINE-3; P < 0,001 in entrambi i casi).
In AMAGINE-1 l'83,3% dei pazienti trattati con 210 mg di brodalumab hanno raggiunto un punteggio PASI di 75, rispetto al 2,7% dei pazienti trattati con placebo (P < 0,001).
Gli eventi avversi più comuni sono stati artralgia, faringite, mal di testa e infezioni delle vie respiratorie superiori Sebbene siano stati registrati casi di ideazioni e comportamenti suicidi, non è stata evidenziata alcuna associazione fra il trattamento con brodalumab e un aumento del rischio di ideazioni e comportamenti suicidi, sottolinea la compagnia. Il lancio di brodalumab in Europa sarà accompagnato da attività di farmacovigilanza per registrare e valutare ogni evento collegato a potenziali rischi per la sicurezza.
Negli Stati Uniti, brodalumab viene venduto con un avvertimento che mette in guardia sul rischio di ideazioni suicide ed è disponibile soltanto attraverso un programma di valutazione e mitigazione del rischio.